
Zulassungserweiterung
für die EREMFAT® Produktpalette*
Seit 2021 ist EREMFAT® (Wirkstoff: Rifcampicin) zugelassen zur Kombinationsbehandlung schwerwiegender grampositiver und gramnegativer nicht-mykobaterieller Infektionen mit Erregerempfindlichkeit gegenüber Rifampicin. Als effektives und schnell wirkendes Biofilm-aktives Antibiotikum kann es dazu beitragen, schwere und langwierige Komplikationen auch für ihre Patienten zu vermeiden. 2, 3
* EREMFAT® 150 mg/300 mg/450 mg/600 mg, Filmtabletten; EREMFAT® i.v. 300 mg/600 mg, Infusionslösung; EREMFAT® Sirup, 100 mg/5 ml,
Granulat zur Herstellung einer Suspension zum Einnehmen

EREMFAT® bei:

Prävalenz
- 437.000 Implantationen von Huft- und Kniegelenkprothesen (2019) 3
- PJI bei 1-4% 2
Krankheitsbild
Die periprothetische Gelenkinfektion (PJI) ist eine ernste Komplikation bei der Implantation von Gelenkersatz, deren Zahl stetig ansteigt. 1, 2 Die PJI tritt bei etwa 1–2 % nach Primär eingriffen und 4 % nach Revisionseingriffen auf. 2
Dazu kommen nicht erkannte chronische Infektionen und das lebenslange Risiko einer PJI durch eine hämatogene Streuung.2
Mikrobiologie
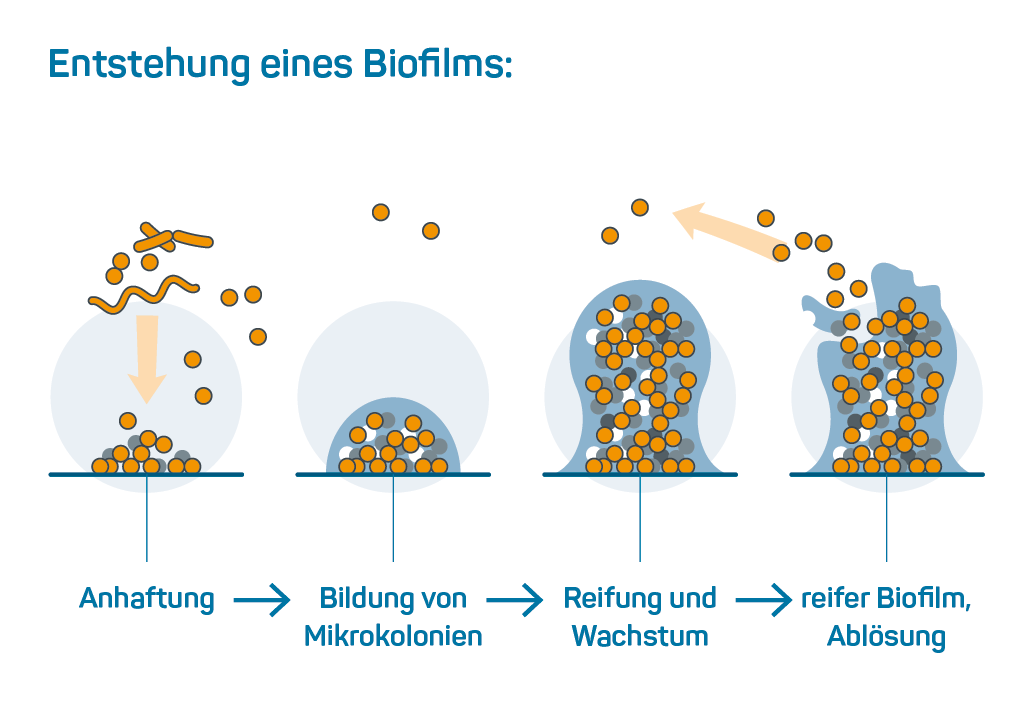
Bei der bakteriellen Besiedelung der Prothese entsteht ein Biofilm, der antibiotisch nur mit Biofilm-aktiven Antibiotika (wie z. B. Rifampicin) zu behandeln ist. Staphylokokken sind die häufigsten Erreger bei PJI. Ein Débridement mit anschließender
Antibiotikagabe kann zu einer erfolgreichen Behandlung der Infektion mit Implantaterhalt führen.4, 5 Als hochvirulenter Keim ist S. aureus vor allem bei der akuten Infektion zu finden, während die koagulase-negativen Staphylokokken (z. B. S. epidermidis) als niedrig virulente Organismen eine subtile, chronische Infektion verursachen.5

Bedeutung von EREMFAT® für die Therapie
- Effektiv gegen die häufigsten Infektionserreger: Staphylococcus aureus (incl. MRSA), Staphylococcus epidermidis 4
- Spielt als Biofilm-aktives Antibiotikum eine Schlüsselrolle für den Therapieerfolg 2, 5, *
- Die Kombinationstherapie mit EREMFAT® (Rifampicin) kann schwerwiegende Komplikationen in der orthopädischen Chirurgie verhindern 5, 6, 7
- Der Einsatz von EREMFAT. (Rifampicin) wird in der PEG S2k- und der IDSA-Leitlinie empfohlen 8, 9, 10
* Voraussetzung ist ein unreifer Biofilm (Infektionsdauer <4 Wochen) und ein vorangegangenes Débridement
Erregerspektrum
EREMFAT® hat eine bakterizide Wirkung gegenüber einer Vielzahl grampositiver und gramnegativer Krankheitserreger; wie Mykobakterien, Meningokokken, Staphylokokken u. a. 3
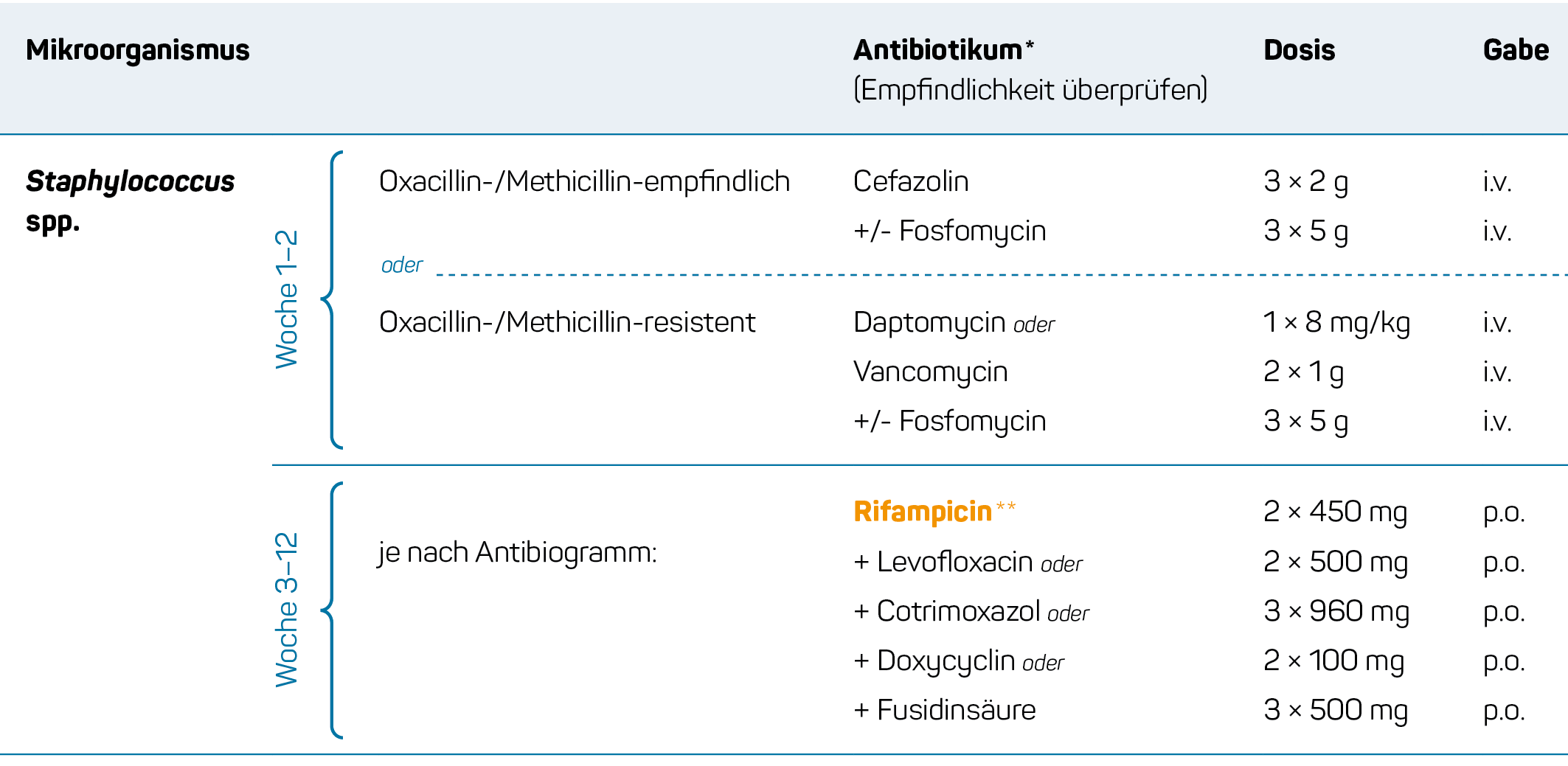
* Therapieschema bei Débridement und Erhalt der Prothese oder einzeitigem Wechsel
** Rifampicin erst nach Prothesen-Wiederaufbau einsetzen. Zur i.v.-Therapie dazugeben, sobald Wundverhältnisse trocken bzw. Drainagen gezogen. Dosisreduktion auf 2 × 300 mg bei Alter >75 J.
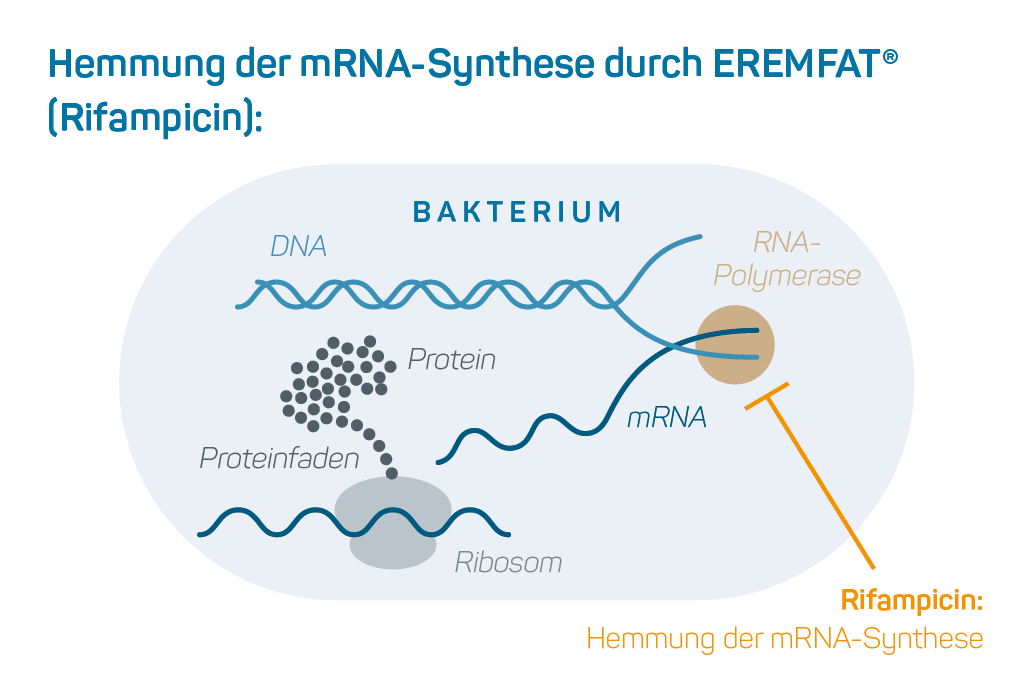
Wirkmechanismus
- Bakterizide Wirkung durch Hemmung der bakteriellen Proteinbiosynthese,
beruhend auf Bindung an die RNA-Polymerase 3 - EREMFAT® ist lipophil und gut gewebegängig 3
- Effektiv gegen Biofilme und intrazelluläre Erreger 2, 3
- Anwendung immer als Kombinationstherapie 3, *
* außer bei Meningitis-Prophylaxe

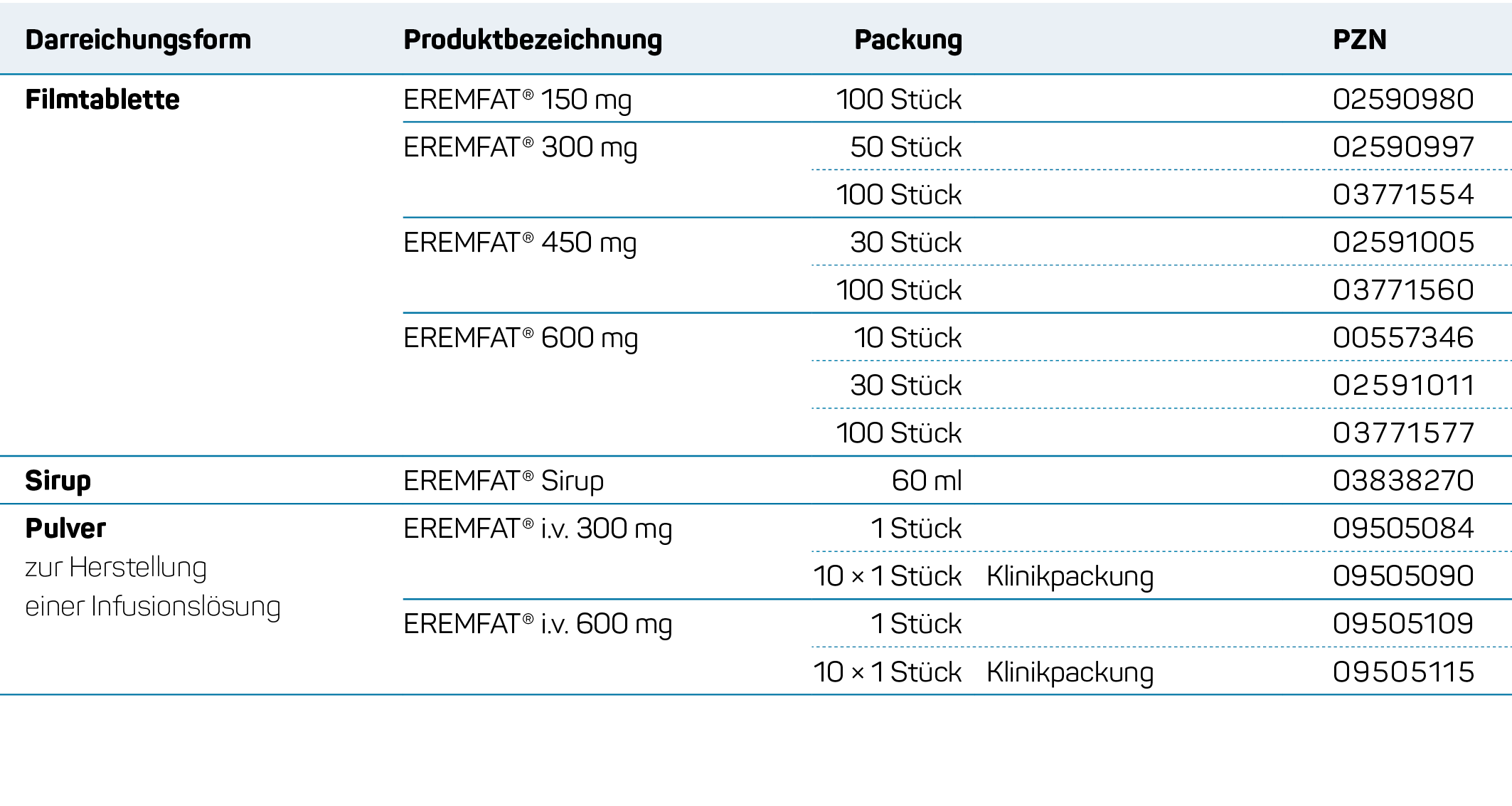
Produktübersicht
QUELLENANGABEN: 1 – Zheng Z, Stewart PS. Antimicrob Agents Chemother. 2002;46(3):900-903. 2 – Zimmerli W, Sendi P. Antimicrob Agents Chemother. 2019;63(2):e01746-18. 3 – Fachinformation EREMFAT® 150 mg/300 mg/450 mg/600 mg, Filmtabletten; EREMFAT® i.v. 300 mg/600 mg, Infusionslösung; EREMFAT® Sirup, 100 mg/5 ml, Granulat zur Herstellung einer Suspension zum Einnehmen (Stand 11.2021). 4 – Mandell GL, Vest TK. J Infect Dis. 1972;125(5):486-490. 5 – Widmer AF et al. Clin Infect Dis. 1992;14(6):1251-1253. 6 – Renz N, Trampuz A. Orthopädie & Rheuma 2015;(18):20-28. 7 – Zimmerli W et al. N Engl J Med 2004;351:1645-54. 8 – El Helou OC et al. Eur J Clin Microbiol Infect Dis. 2010;29(8):961-967. 9 – PEG S2K Leitlinie, Kalkulierte parenterale Initialtherapie bakterieller Erkrankungen bei Erwachsenen – Update 2018, AWMF Registernummer 082 – 006, www.awmf.org/leitlinien/detail/ll/082-006.html. 10 – RKI-Ratgeber 2016 – Staphylokokken-Erkrankungen, insbesondere Infektionen durch MRSA https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Staphylokokken_MRSA.html. 11 – Osmon DR et al. Clin Infect Dis. 2013;56(1):e1-e25. 12 – Galar A et al. Clin Microbiol Rev 2019;32(2):e00041-18. 13 – Habib G et al. Eur Heart J 2015 Nov;36(44):3075-128. 14 – Coiffier G et al. Joint Bone Spine. 2013;80(1):11-17. 15 – Waldvogel FA et al. N Engl J Med. 1970;282(4):198-206. 16 – Berbari EF et al. Clin Infect Dis. 2015;61(6):e26-e46. 17 – Liu C et al. Clin Infect Dis. 2011;52(3):e18–e55. 18 – Pocket Guide zur Diagnostik und Behandlung von periprothetischen Infektionen, Version 10 (Oktober 2021), www.pro-implant.org.
